高中化学电解池知识考点汇总
请您在阅读本文之前,点击右上角的“关注”,以后您就可以免费收到吃货界最佳仙女每天推送的高中各科知识点最新内容了。如有问题请私信小编,谢谢您的关注与转发!
知识考点一 电解的原理
1.电解定义
在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程。
2.能量转化形式
电能转化为化学能。
3.电解池
(1)构成条件
①有与电源相连的两个电极。
②电解质溶液(或熔融盐)。
③形成闭合回路。
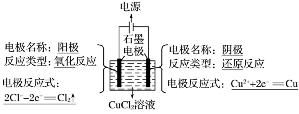
(2)电极名称及电极反应式(如图)
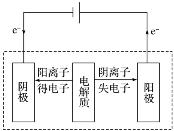
(3)电子和离子的移动方向
特别注意: 电解时,在外电路中有电子通过,而在溶液中是依靠离子定向移动形成电流,即电子本身不会通过电解质溶液。
4.分析电解过程的思维程序
(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。
(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组(不要忘记水溶液中的H+和OH-)。
(3)然后排出阴、阳两极的放电顺序
阴极:阳离子放电顺序:
Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+。
阳极:
活泼电极>S2->I->Br->Cl->OH->含氧酸根离子。
(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷守恒。
(5)最后写出电解反应的总化学方程式或离子方程式。
注意点:
1.做到“三看”,正确书写电极反应式
(1)一看电极材料,若是金属(Au、Pt除外)作阳极,金属一定被电解(注Fe生成Fe2+)。
(2)二看介质,介质是否参与电极反应。
(3)三看电解质状态,若是熔融状态,就是金属的电冶炼。
2.规避“三个”失分点
(1)书写电解池中电极反应式时,要以实际放电的离子表示,但书写总电解反应方程式时,弱电解质要写成分子式。
(2)要确保两极电子转移数目相同,且应注明条件“电解”。
(3)电解水溶液时,应注意放电顺序中H+、OH-之后的离子一般不参与放电。
知识考点二 电解原理的应用
1.电解饱和食盐水
(1)电极反应
阳极反应式:2Cl--2e-===Cl2↑(氧化反应)
阴极反应式:2H++2e-===H2↑(还原反应)
(2)总反应方程式
2NaCl+2H2O电解2NaOH+H2↑+Cl2↑
离子反应方程式:2Cl-+2H2O电解2OH-+H2↑+Cl2↑
(3)应用:氯碱工业制烧碱、氯|气和氢气。
2.电镀
以金属表面镀银为例,
(1)镀件作阴极,镀层金属银作阳极。
(2)电解质溶液是AgNO3溶液等含镀层金属阳离子的盐溶液。
(3)电极反应:
阳极:Ag-e-===Ag+;
阴极:Ag++e-===Ag。
(4)特点:阳极溶解,阴极沉积,电镀液的浓度不变。
3.电解精炼铜
(1)电极材料:阳极为粗铜;阴极为纯铜。
(2)电解质溶液:含Cu2+的盐溶液。
(3)电极反应:
阳极:
Zn-2e-===Zn2+
Fe-2e-===Fe2+
Ni-2e-===Ni2+
Cu-2e-===Cu2+;
阴极:
Cu2++2e-===Cu。
4.电冶金
利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
(1)冶炼钠
2NaCl(熔融)电解2Na+Cl2↑
电极反应:
阳极:
2Cl--2e-===Cl2↑;
阴极:
2Na++2e-===2Na。
(2)冶炼铝
2Al2O3(熔融)==4Al+3O2↑(条件:通电)
电极反应:
阳极:6O2--12e-===3O2↑;
阴极:4Al3++12e-===4Al。
知识考点三 应对电化学定量计算的三种方法
1.计算类型
原电池和电解池的计算包括两极产物的定量计算、溶液pH的计算、相对原子质量和阿伏加德罗常数的计算、产物的量与电量关系的计算等。
2.三种方法
(1)根据总反应式计算
先写出电极反应式,再写出总反应式,最后根据总反应式列出比例式计算。
(2)根据电子守恒计算
①用于串联电路中阴阳两极产物、正负两极产物、相同电量等类型的计算,其依据是电路中转移的电子数相等。
②用于混合溶液中电解的分阶段计算。
(3)根据关系式计算
根据得失电子守恒定律关系建立起已知量与未知量之间的桥梁,构建计算所需的关系式。
如以通过4 mol e-为桥梁可构建如下关系式:
阳极产物 阴极产物
(式中M为金属,n为其离子的化合价数值)
该关系式具有总揽电化学计算的作用和价值,熟记电极反应式,灵活运用关系式便能快速解答常见的电化学计算问题。
提示:在电化学计算中,还常利用Q=I・t和Q=n(e-)×NA×1.60×10-19来计算电路中通过的电量。
知识考点四 金属的腐蚀和防护
1.金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2.金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
类型
化学腐蚀
电化学腐蚀
条件
金属跟非金属单质直接接触
不纯金属或合金跟电解质溶液接触
现象
无电流产生
有微弱电流产生
本质
金属被氧化
较活泼金属被氧化
联系
两者往往同时发生,电化学腐蚀更普遍
(2)析氢腐蚀与吸氧腐蚀
以钢铁的腐蚀为例进行分析:
类型
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较强(pH≤4.3)
水膜酸性很弱或呈中性
负极反应
Fe-2e-===Fe2+
Fe-2e-===Fe2+
正极反应
2H++2e-===H2↑
O2+2H2O+4e-===4OH
总反应
Fe+2H+===Fe2++H2↑
2Fe+O2+2H2O===2Fe(OH)2
联系
吸氧腐蚀更普遍
3.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法―原电池原理
a.负极:比被保护金属活泼的金属;
b.正极:被保护的金属设备。
②外加电流的阴极保护法―电解原理
a.阴极:被保护的金属设备;
b.阳极:惰性金属或石墨。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
注意点:
1.判断金属腐蚀快慢的规律
(1)对同一电解质溶液来说,腐蚀速率的快慢:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防腐措施的腐蚀。
(2)对同一金属来说,在不同溶液中腐蚀速率的快慢:强电解质溶液中>弱电解质溶液中>非电解质溶液中。
(3)活动性不同的两种金属,活动性差别越大,腐蚀速率越快。
(4)对同一种电解质溶液来说,电解质浓度越大,金属腐蚀越快。
2.两种保护方法的比较
外加电流的阴极保护法保护效果大于牺牲阳极的阴极保护法。
文章来源互联网,感谢原创,免费分享,如有侵权请联系删除
相关文章
-

高中化学易错类型专题突破―氧化还原反应
高中化学易错类型专题突破―氧化还原反应
-

高二化学期末试题送到,孜孜不倦,必有好成绩
高二的试题其实只是比高三少了有机化学部分,高三党也可以做一做,后面附有答案,希望对大家有用。还是那句话,晓琼老师只为大家服务,话不多说,看题:后面..
-
高中化学知识点总结氧化性、还原性强弱的判断
高中化学知识点总结:氧化性、还原性强弱的判断(1)根据元素的化合价物质中元素具有最高价,该元素只有氧化性;物质中元素具有最低价,该元素只有还原性;物..
猜你喜欢
-
重庆十一中2016年高二上数学文期中试题含答案
重庆十一中高2018级高二( 上)半期考试数学(文科)试题考试说明:1.考试时间 120分钟 2.试题总分 150分一、选择题:(本题共12小题,每小题5分,共60分,在..
-
女厕所不用打扫
1、上高三的时候,为了备考,保养身体,老师规定每天早上一袋奶,上早自习的时候,我后面的女生给我一袋奶,让我放在旁边的暖气上热一下。早自习结束后,这姑..
-
兔子打伞
1、儿子:爸爸 老师今天说我,有其父必有其子 这是什么意思啊?爸爸:(暴跳如雷的)快说 你今天又干什么坏事了?2、饭店广告---你不来吃饭,我们就会饿着肚子..
-
高考将至,生物有哪些技巧?
用对的学习方法和学习技巧来学习,成绩自然就会提高,还好,有清华北大的伙伴们编写的《疯狂600提分笔记》解读高考出题规律,答题技巧,应试技巧等。对于理科..
-
别人都骂不过我了
1、最初打网游的时候因为技术不好,被人骂成狗。还好后来有大神带我一起玩,我虚心请教,学到了很多经验。现在的我终于和从前大不一样了。。。别人都骂不过我..


