高一化学氨硝酸硫酸专题突破训练
硝酸是一种具有强氧化性、腐蚀性的强酸,属于一元无机强酸。接下来我们大家一起练习高一化学氨硝酸硫酸专题突破训练。
1.含H原子个数为1.806×1023个NH3,其质量为( )
A.17克 B.0.17克
C.1.7克 D.5.4克
【解析】 n(H)=1.806×10236.02×1023=0.3 mol,n(NH3)=nH3=0.1 mol,故C正确。
【答案】 C

2.下列性质不属于氨气的物理性质的是( )
A.易液化 B.极易溶于水
C.水溶液显碱性 D.有刺激性气味
【解析】 氨气溶于水得氨水,其水溶液呈碱性的原因是由于NH3与水发生了反应,生成NH3H2O,NH3H2ONH+4+OH-,所以这是NH3的化学性质。
【答案】 C
3.下面的反应中,氨作为氧化剂参加反应的是( )
A.NH3+H3PO4===NH4H2PO4
B.2NH3+2Na===2NaNH2+H2
C.8NH3+3Cl2===6NH4Cl+N2
D.4NH3+5O2=====催化剂△4NO+6H2O
【解析】 氨作为氧化剂参加反应时为NH3分子中氢的化合价降低。此题涉及的反应较为特殊。
【答案】 B
4.(双选)下列离子方程式正确的是( )
A.实验室制NH3:NH+4+OH-=====△NH3↑+H2O
B.NaOH与NH4Cl溶液混合加热:NH+4+OH-=====△NH3H2O
C.氨水中加盐酸:NH3H2O+H+===NH+4+H2O
D.氨气通入稀H2SO4中:NH3+H+===NH+4
【解析】 实验室制NH3用的是NH4Cl固体与消石灰反应,属于固体之间的反应,不能用离子方程式表示,所以A项不正确。NaOH和NH4Cl溶液混合加热产生NH3,离子方程式应为NH+4+OH-=====△NH3↑+H2O,故B项也不正确。
【答案】 CD
5.检验铵盐溶液的方法是:将待测物质取出少量,放在试管中,然后( )
A.加热,用湿润的红色石蕊试纸置于试管口检验
B.加强碱溶液后加热,再滴入无色酚酞试液
C.加热,用蘸有浓盐酸的玻璃棒置于试管口检验
D.加烧碱溶液后加热,再用湿润的红色石蕊试纸置于试管口检验
【解析】 检验铵盐与碱共热放出碱性气体,使指示剂变色的方法。A、C错,并非所有铵盐加热分解都产生NH3。B错,加碱共热后,NH3已跑出。
【答案】 D

6.无色的混合气体甲中可能含NO、CO2、NO2、NH3、N2中的几种。将100 mL气体甲经过下图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
A.NH3、NO2、N2 B.NH3、NO、CO2
C.NH3、NO2、CO2 D.NO、CO2、N2
【解析】 无色气体中不含NO2;通过浓H2SO4时,气体体积减少20 mL,说明含有NH3;通过Na2O2后气体显红棕色,说明含有CO2和NO,在通过Na2O2时,CO2与Na2O2反应产生O2,NO再与O2反应生成红棕色的NO2气体;NO2和O2按41的体积比通入H2O中时可被完全吸收。
【答案】 B
高中是人生中的关键阶段,大家一定要好好把握高中,小编为大家整理的高一化学氨硝酸硫酸专题突破训练,希望大家喜欢。
温馨提醒:
想要收藏更多高中各学科知识点与学习方法,请关注头条号【求知学园】
欢迎 转发给更多有需要的朋友以及同学们!
相关文章
-

高中化学易错类型专题突破―氧化还原反应
高中化学易错类型专题突破―氧化还原反应
-

高二化学期末试题送到,孜孜不倦,必有好成绩
高二的试题其实只是比高三少了有机化学部分,高三党也可以做一做,后面附有答案,希望对大家有用。还是那句话,晓琼老师只为大家服务,话不多说,看题:后面..
-
高中化学知识点总结氧化性、还原性强弱的判断
高中化学知识点总结:氧化性、还原性强弱的判断(1)根据元素的化合价物质中元素具有最高价,该元素只有氧化性;物质中元素具有最低价,该元素只有还原性;物..
猜你喜欢
-

关注!海南2017级高中生今年秋季开始“选课走班”
2017年,海南省启动高考改革,也就是2017年秋季学期入学的高一学生,将面临新的高考模式。高考改革赋予了普通高中学生对于学习科目的选择权。26日,记者从省..
-

高考物理知识点梳理(最全)
-
爆笑:有了老婆,经常让人受刺激
1、翻开老婆的钱包:农行卡、建行卡、邮政卡、还有我的工资卡。。。再看看我的钱包:天然气卡、水费、电费卡、超市积分卡、饭馆会员打折卡。。。2、老婆出门..
-

高中生物思维导图
-
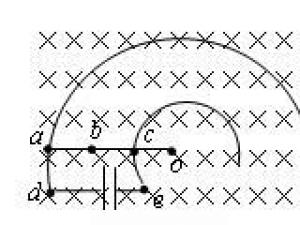
资深物理老教师教你如何巧抓高考物理题中漏洞,快速破析选择题
有些选择题的"漏洞"出在基础知识上,主要体现在对基础知识误用或错用,对规律定理的理解不到位,对元件特性不清楚等方面。例1(2009福建高考)(多..


