电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等
今天小瑞老师给大家带来的复习专题是高中化学电荷守恒与物料守恒,并且根据同学们的需要给大家一些练习题,希望大家可以多多练习。电荷守恒和物料守恒知识点
1.电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。如NaHCO3溶液中:n(Na+)+n(H+)=n(HCO3-)+2n(CO32-)+n(OH-)推出:
c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
2.物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。如NaHCO3溶液中n(Na+):n(c)=1:1,推出:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
3.导出式――质子守恒:
如碳酸钠溶液中由电荷守恒和物料守恒将Na+离子消掉可得:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。
如醋酸钠溶液中由电荷守恒和物料守恒将钠离子消掉可:c(OH-)=c(H+)+c(CH3COOH)。
[规律总结]正确的思路:

【常见题型】
一、溶质单一型――关注三个守恒
1.弱酸溶液:
【例1】在0.1mol/L的H2S溶液中,下列关系错误的是( )
A.c(H+)=c(HS-)+c(S2-)+c(OH-) B.c(H+)=c(HS-)+2c(S2-)+c(OH-)
C.c(H+)>[c(HS-)+c(S2-)+c(OH-)] D.c(H2S)+c(HS-)+c(S2-)=0.1mol/L
分析:由于H2S溶液中存在下列平衡:H2S

H++HS-,HS-

H++S2-,H2O

H++OH-,根据电荷守恒得c(H+)=c(HS-)+2c(S2-)+c(OH-),由物料守恒得c(H2S)+c(HS-)+c(S2-)=0.1mol/L,所以关系式错误的是A项。
(注意:解答这类题目主要抓住弱酸的电离平衡。)
2.弱碱溶液:
【例2】室温下,0.1mol/L的氨水溶液中,下列关系式中不正确的是( )
A. c(OH-)>c(H+) B.c(NH3・H2O)+c(NH4+)=0.1mol/L
C.c(NH4+)>c(NH3・H2O)>c(OH-)>c(H+) D.c(OH-)=c(NH4+)+c(H+)
分析:由于氨水溶液中存在一水合氨的电离平衡和水的电离平衡,所以所得溶液呈碱性,根据电荷守恒和物料守恒知BD正确,而一水合氨的电离是微量的,所以C项错误,即答案为C项。
3.强酸弱碱盐溶液:
【例3】在氯化铵溶液中,下列关系正确的是( )
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.c(NH4+)=c(Cl-)>c(H+)=c(OH-) D.c(Cl-)=c(NH4+)>c(H+)>c(OH-)
分析:由于氯化铵溶液中存在下列电离过程:NH4Cl=NH4++Cl-,H2O

H++OH-和水解过程:NH4++H2O

H++NH3・H2O,由于NH4+水解被消耗,所以c(Cl-)>c(NH4+),又因水解后溶液显酸性,所以c(H+)>c(OH-),且水解是微量的,所以正确的是A项。(注意:解答这类题时主要抓住弱碱阳离子的水解,且水解是微量的,水解后溶液呈酸性。)
4.强碱弱酸盐溶液:
【例4】在Na2S溶液中下列关系不正确的是
A. c(Na+) =2c(HS-) +2c(S2-) +c(H2S) B.c(Na+) +c(H+)=c(OH-)+c(HS-)+2c(S2-)
C.c(Na+)>c(S2-)>c(OH-)>c(HS-) D.c(OH-)=c(HS-)+c(H+)+c(H2S)
解析:电荷守恒:c(Na+) +c(H+)=c(OH-)+c(HS-)+2c(S2-);
物料守恒:c(Na+) =2c(HS-) +2c(S2-) +2c(H2S);
质子守恒:c(OH-)=c(HS-)+c(H+)+2c(H2S),选A D
5.强碱弱酸的酸式盐溶液:
【例5】(2004年江苏卷)草酸是二元弱酸,草酸氢钾溶液呈酸性,在0.1mol/LKHC2O4溶液中,下列关系正确的是(CD)
A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+ c(C2O42-) B.c(HC2O4-)+ c(C2O42-)=0.1mol/L
C.c(C2O42-)>c(H2C2O4) D.c(K+)= c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)
分析:因为草酸氢钾呈酸性,所以HC2O4-电离程度大于水解程度,故c(C2O42-)>c(H2C2O4)。又依据物料平衡,所以D.c(K+)= c(H2C2O4)+ c(HC2O4-)+ c(C2O42-)正确,又根据电荷守恒:c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-),所以综合上述C、D正确。

习题练习
1、(2001年全国春招题)在0.1mol・L-1 Na2CO3溶液中,下列关系正确的是( )。
A.c(Na+)=2c(CO32-
B.c(OH-)=2c(H+)
C.c(HCO3-)>c(H2CO3)
D.c(Na+)<c(CO32-)+c(HCO3-)
2、在0.1mol/L的NaHCO3溶液中,下列关系式正确的是( )
A.c(Na+)>c(HCO3-)>c(H+)>c(OH-)
B.c(Na+)=c(HCO3-)>c(OH-)>c(H+)
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
3、 已知某温度下0.1mol・L-1的NaHB(强电解质)溶液中c(H+)>c(OH-),则下列有关说法或关系式一定正确的是( )
①HB-的水解程度小于HB-的电离程度;②c(Na+)=0.1mol・L-1 ≥c(B2-);
③溶液的pH=1;④c(Na+)=c(HB-)+2c(B2-)+c(OH-)。
A.①② B.②③ C.②④ D.①②③
4、(2006江苏)1、下列叙述正确的是( )
A.0.1mol・L-1氨水中,c(OH-)=c(NH4+)
B.10 mL 0.02mol・L-1HCl溶液与10 mL 0.02mol・L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
C.在0.1mol・L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
D.0.1mol・L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
5、(05上海)14、叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是( )
A、HN3水溶液中微粒浓度大小顺序为:c(HN3)>c(H+)>c(N3)>c(OH)
B、HN3与NH3作用生成的叠氮酸铵是共价化合物
C、NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N3) >c(OH)>c(H+)
D、N3与CO2含相等电子数
Tags:物料 电解质 正电荷 负电荷 阴离子 阳离子 单一型
相关文章
-
2025-09-10
高考化学选择题满分攻略 七个题型三个步骤妥妥拿满分!
要想化学考试拿高分,选择题非常重要。往年高考都突出化学主干知识的考查,如:氧化还原反应、离子反应、热化学、阿伏加德罗常数、元素周期律、电化学、化学反应速率和化学平衡等。那么,化学的选择题要怎么做才能拿高分呢?万朋教育小编结合化学选择题的特点和类型,谈一谈如何利用三步突破化学选..
-
2025-07-30
高二化学复习中需注意的25个考点
25个化学考试中的常见知识点高中学习网为大家罗列了25个化学考试中的常见知识点,在进行化学复习的过程中,应予以重视,一下是具体内容。以下是高考常见的考点:1)阿伏加德罗常数;2)氧化还原反应;3)离子反应、离子方程式;4)溶液、离子浓度及其转变;5)“位一构―性”,即元素在周期表中的位置、原子..
-
2025-07-24

2018年高考化学试题预测
未考先知――2018年高考化学全国卷信息归集与高考命题预测一、高考信息归集1.试卷结构2018年试卷结构不发生变化。2.考核目标与要求2018年考核目标与要求不发生变化,保持了全国卷的稳定性,在复习备考中,应多关注近两年考试说明中变化的内容。主要梳理如下:(1)加强“化学符号对应物理量的认知”..
猜你喜欢
-
2018-08-19
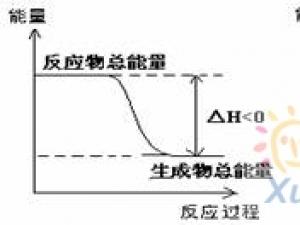
能量变化两种图像的考查
化学反应的能量变化取决于反应物和生成物具有的总能量的相对大小,取决于发生反应破坏旧的化学键吸收的能量与形成新的化学键放出能量的相对大校这是理解化学反应热效应的两种角度,如放热反应可以分别表示为图中两种图像:08的两道高考题正是通过这两种图像形式对能量变化知识点进行了考查。(08全..
-
2018-11-14
要确保养的小鸟飞不出去
1、商场里。女:“相中没?”男:“没1女:“那你就别摸,很贵的1............可能你们和我一样以为这是顾客与营业员的对话,其实TM这是一对狗男女在哪里相亲。@biao521ge2、本人打算购房了,咱可不差钱,为了彰显土豪本色,我对卖家提出四点要求:第一是房子的通风透光必须好;第二是房子必须是..
-
2020-01-30

交际花学妹,长得漂亮,身材高挑
上高中的时候我有个交际花学妹,长得漂亮,身材高挑,人堆一放,特别扎眼的那一种,但是性格很好,说是交际花,其实单纯得很,不过是朋友众多。学妹刚一进高一,就一帮人蜂拥而至,使出浑身解数想要追到她但是学妹选了一个小混混。小混混每天不学无术,惶惶度日,但仗着一米八的身高和一张还算可以..
-
2025-07-03
女人是水做的
1、女人如衣服。女朋友是风衣:飘忽不定,上下翻飞。妻子是内衣:贴身又贴心。小三是外套:外套要外穿,回到家里就得脱。情人是休闲装:外出娱乐休闲、消遣、或放松,就会套上休闲装。女秘书是西装:笔挺、锃亮,穿在身上,很有面子,有尊严。郑重提醒:衣服千万别乱穿。2、女人是水做的,为了迎合..
-
2018-10-24
今天放学有三个女孩追我
1、做生意亏了本,去找朋友借钱准备东山再起。儿子写完了作业,我同意带他一起前往。朋友听了我的情况后,很爽快地取出2万元给我。我向他保证:“做事不能再盲目,要多动脑筋,把钱用在刀刃上。”回家后,没等我将此事告诉老婆,儿子便抢先道:“妈妈。给你说个不好的消息,爸爸准备买刀。”2、儿子..